Estamos cercados de radiação 24 horas por dia. A luz que chega até seus olhos, um sinal de Wi-Fi, o LED de um controle remoto, uma máquina de tomografia, são todos exemplos de radiação. Naturalmente, uma radiação de um sinal de Wi-Fi tem muito menos energia do que os raios ultravioleta do Sol, e que este tem muito menos energia do que uma máquina de tomografia — e é exatamente esse o ponto! Esse nível de energia é o que determina se uma radiação é ionizante ou não-ionizante.
Mas o que é “ionizante”?
Ionização de átomos e moléculas
Um átomo é formado por prótons, nêutrons e elétrons. Para formar moléculas, os átomos se ligam com outros átomos por meio do compartilhamento de elétrons, a chamada ligação covalente, ou cedendo/tomando elétrons de outros átomos, a ligação iônica. Portanto, os elétrons têm um papel fundamental na estabilidade do átomo e das moléculas.
Quando um elétron é arrancado de um átomo, a balança se desequilibra e temos mais prótons do que elétrons. Por isso, um átomo de sódio (Na) que perdeu um elétron é chamado de Na+. Esse ato de “perder elétrons” é o que chamamos de ionização. Um átomo se torna ionizado quando perde um ou mais elétrons, e isso altera sua capacidade de formar ligações moleculares.
Portanto, uma radiação ionizante é um tipo de radiação que tem energia o suficiente para arrancar elétrons dos átomos, quebrando ou alterando as ligações moleculares (radiólise) — como a radiação alfa do urânio ou a radiação gama. E por que isso é perigoso?
Nosso corpo é formado por inúmeras moléculas complexas que desempenham um papel fundamental, as principais delas sendo o DNA e o RNA. Quebrar ou danificar as moléculas de DNA e RNA podem trazer mutações genéticas e problemas de saúde gravíssimos e, em muitos casos, irreversíveis.
Por outro lado, a radiação não-ionizante, como a que convivemos no dia-a-dia, não tem energia suficiente para perturbar os elétrons dos átomos — mas nem por isso deixam de ser perigosas em grandes intensidades, como veremos logo mais.
Tipos de radiação
Quando falamos em “radiação”, podemos nos referir a um dos dois principais tipos de radiação. Existe radiação formada por partículas subatômicas (diretamente ionizantes), e a radiação eletromagnética (indiretamente ionizantes). Vamos falar sobre cada uma delas.
Radiação diretamente ionizante: as partículas alfa e beta
A radiação formada por partículas subatômicas pode ser constituída por partículas alfa, partículas beta ou nêutrons. Em essência, são “pedaços” de átomos viajando em alta velocidade devido ao decaimento radioativo e quase todos são ionizantes devido à interação física entre as partículas.
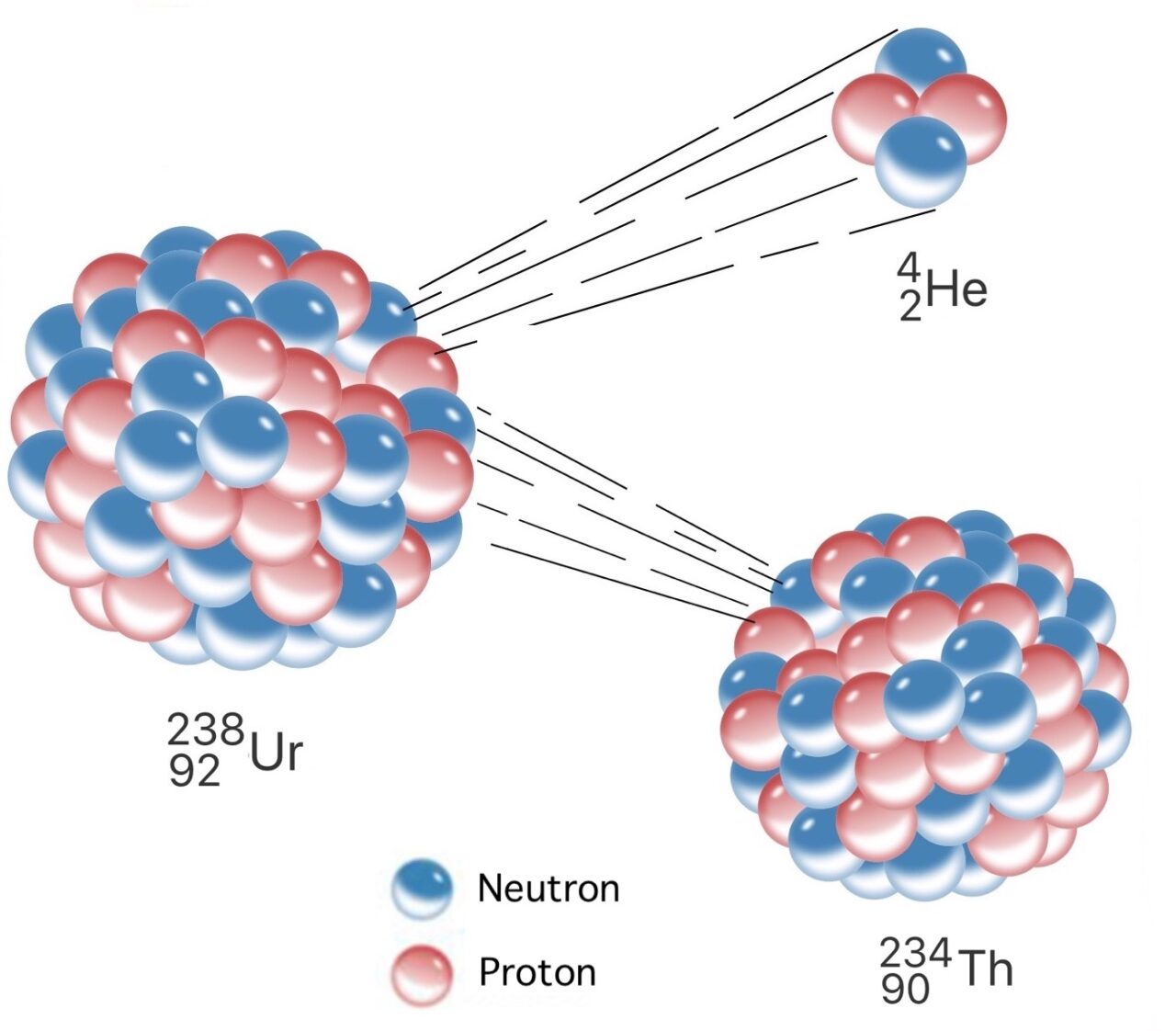
A radiação alfa se consiste na emissão de um núcleo contendo dois prótons e dois nêutrons (idêntico ao núcleo de hélio) devido ao decaimento alfa. Um núcleo instável de urânio-238 pode sofrer decaimento alfa, perder dois prótons e dois nêutrons, se transformando em tório-234.
As partículas alfa são emitidas espontaneamente por elementos radioativos, como urânio, polônio e rádio. Essas partículas alfa são grandes e emitidas em alta velocidade. Ao colidirem com outros átomos e moléculas (como as do nosso corpo), a energia cinética da colisão leva à ionização desses átomos, como se estivessem sendo bombardeados — motivo pela qual manipular elementos radioativos é extremamente perigoso. Os raios cósmicos também são partículas alfa, mas são filtrados ao colidirem com as moléculas da atmosfera da Terra, transformando-os em múons.

A radiação beta é um elétron ou pósitron (anti-elétron) e um neutrino devido ao decaimento beta — a transformação de um próton em um nêutron, ou um nêutron em um próton. Essas partículas beta são ejetadas em velocidades relativísticas, de forma que a energia cinética tem o poder de ionizar outros átomos.
Nem a partícula beta, nem seu (anti-)neutrino associado existem dentro do núcleo antes do decaimento beta, mas são criados no processo de decaimento. Um exemplo é o decaimento do carbono-14. O carbono-14 é radioativo, pois um de seus nêutrons pode se decair em um próton, transformando-o em um átomo de nitrogênio-14.
Radiação indiretamente ionizante: a radiação eletromagnética
A radiação eletromagnética pode ser dividida em diversas regiões do chamado espectro eletromagnético. As radiações de baixa energia (e longos comprimentos de onda) no lado das ondas de rádio e micro-ondas; e as radiações de alta energia (e curtos comprimentos de onda) no lado dos raios gama e raios X.

A radiação ionizante indireta interage com a matéria de uma forma que não causa diretamente a ionização por meio de sua interação inicial. Em vez disso, inicia processos que levam à ionização de átomos ou moléculas. Os principais mecanismos pelos quais a radiação de fótons leva à ionização indireta são o efeito fotoelétrico, o espalhamento Compton e a produção de pares.
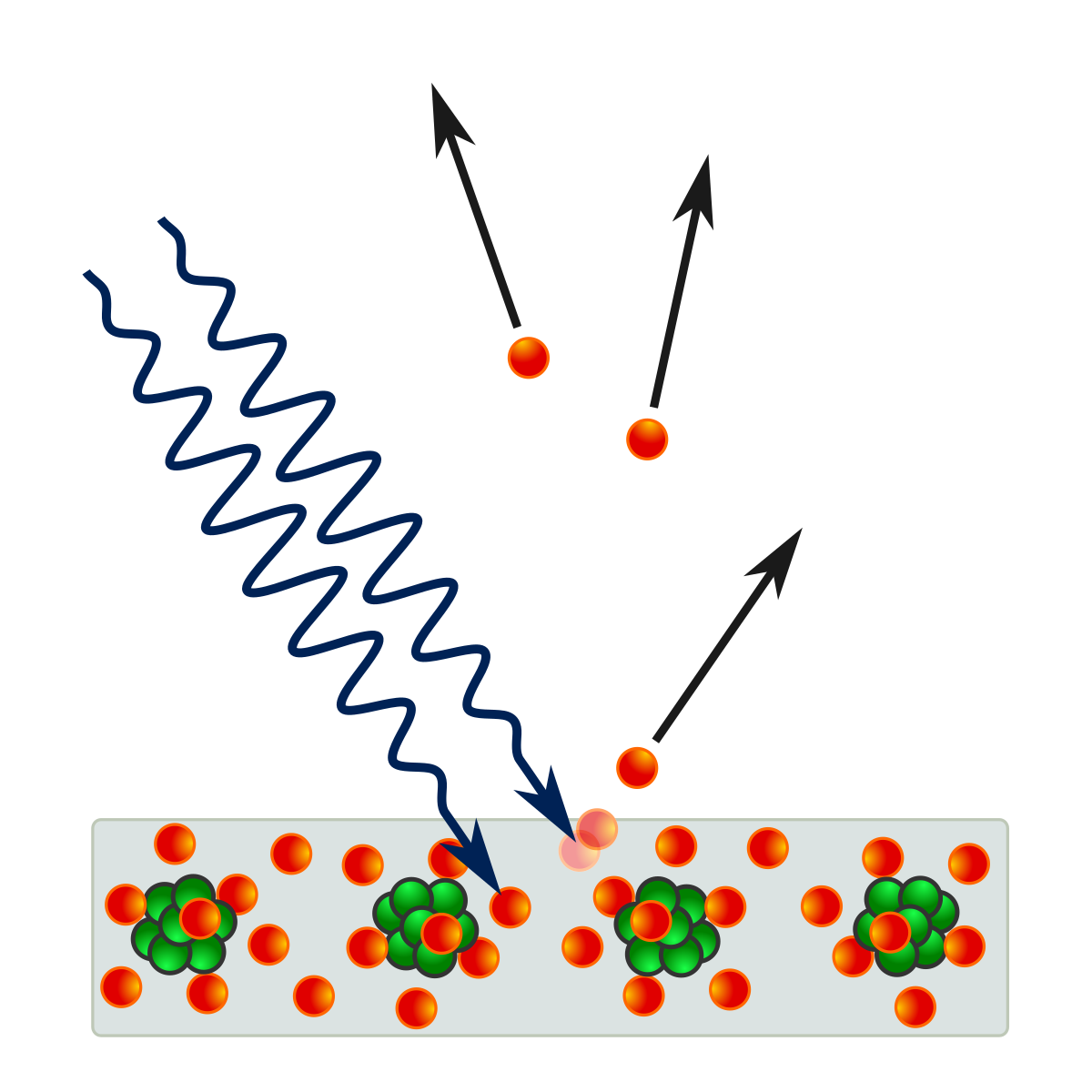
No efeito fotoelétrico, um fóton atinge um átomo e é completamente absorvido, ejetando um elétron de uma das camadas desse átomo. A energia do fóton é parcialmente usada para superar a energia de ligação do elétron, e o restante é transmitido ao elétron como energia cinética. Este processo ioniza diretamente o átomo e o elétron ejetado pode ionizar ainda mais outros átomos à medida que se desloca através do material.
O espalhamento Compton ocorre quando um fóton de alta energia (como raios X) colide com um elétron num átomo. Parte da energia do fóton é transmitida ao elétron, e a parte restante é refletida. O elétron ejetado de seu orbital tem energia cinética suficiente para causar mais ionizações no material. Enquanto isso, o fóton espalhado, agora com energia mais baixa, pode sofrer mais espalhamentos Compton ou outras interações até que sua energia esteja suficientemente esgotada.
A produção de pares é um processo que ocorre quando um fóton de raios gama (com energia superior a 1,022 MeV) passa próximo ao núcleo de um átomo, interage com seu campo elétrico e se transforma em um par elétron-pósitron. A energia do fóton é convertida na massa dessas duas partículas, com qualquer energia restante transmitida como energia cinética ao par. Tanto o elétron quanto o pósitron podem causar mais ionizações à medida que diminuem a velocidade. Eventualmente, o pósitron se aniquilará com um elétron, produzindo dois fótons gama que podem continuar a cadeia de interações, levando a mais ionizações indiretas.
Radiação não-ionizante
Os fótons da região inferior do espectro eletromagnético não têm energia suficiente para perturbar os elétrons dos átomos e, portanto, são chamadas de radiações não-ionizantes. Apesar das radiações não-ionizantes não produzirem efeitos mutagênicos (que podem levar ao câncer), em grandes intensidades elas podem ser percebidas como energia térmica e causar queimaduras, motivo pela qual existem normas regulatórias para a radiofrequência.
Essa região do espectro contempla as ondas de rádio, o micro-ondas, o infravermelho, a luz visível e uma parte do ultravioleta-próximo (ou UV-A).

Um sinal de celular, como 4G ou 5G, faz uso das ondas eletromagnéticas na região do micro-ondas (de 700 a 2100 MHz), isso significa que esses fótons têm até menos energia do que o infravermelho ou luz visível. Essas ondas são longas e atravessam nosso corpo como se fôssemos transparentes, sem causar dano algum.
A radiação infravermelha, apesar de não-ionizante, tem um comprimento de onda similar ao tamanho de uma molécula, portanto, é capaz de agitá-las. Percebemos a vibração e agitação molecular como calor e, por isso, o infravermelho é considerado também uma radiação térmica. O infravermelho, apesar de não-ionizante, pode ser perigoso devido ao risco de queimaduras causado pela radiação térmica.
Naturalmente, a luz visível é inofensiva para nós em doses moderadas. Apesar de não-ionizante, quando focadas ou em grande intensidade podem causar queimaduras e danos aos materiais sólidos e tecidos orgânicos, como é o caso do laser.

Já o ultravioleta-próximo (UV-A) é um caso especial. Embora tecnicamente não-ionizante, ainda pode excitar e causar reações fotoquímicas em algumas moléculas. Isso acontece porque nas energias do ultravioleta, as moléculas podem ficar eletronicamente excitadas ou promovidas à forma de radical livre, mesmo sem ocorrer a ionização. Uma vez que estas reações são, muitas vezes, muito semelhantes às causadas pela radiação ionizante, todo o espectro UV pode ser considerado equivalente à radiação de ionização na sua interação (principalmente tecidos orgânicos).
Apesar de perigosas, as radiações ionizantes podem ser benéficas à civilização moderna quando dominadas e controladas: as máquinas de radiografias e tomografias usam os raios X para diagnóstico por imagem; a tomografia por emissão de pósitron (PET) usa o decaimento beta dos elementos radioativos; os detectores de fumaça funcionam por meio do decaimento alfa do amerício-241; a radiação gama alimenta os reatores de fissão nuclear para geração de energia; o UV-A do Sol faz parte dos processos fotoquímicos para a produção da vitamina D.
Claro, apesar de benéfica, a exposição ao Sol deve ser feita com moderação. Sempre use filtro solar e óculos escuros.